FACTORES QUE AFECTAN LA VELOCIDAD DE REACCION

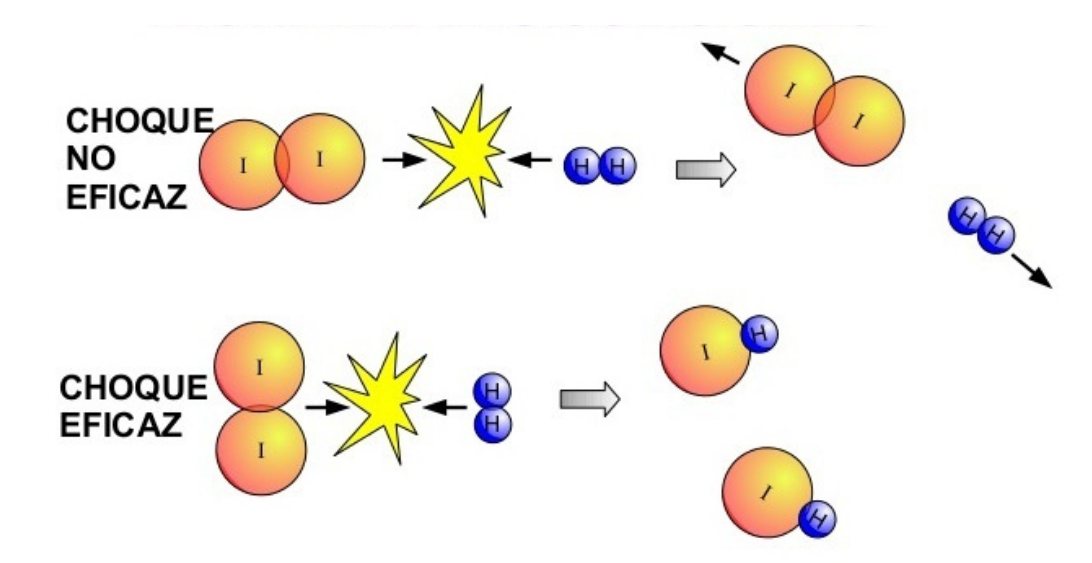
Según con la teoría de colisiones, la velocidad de reacción depende de las colisiones efectivas entre las partículas de los reactivos.
Los principales factores que afectan son:
Estado de agregación de la materia y concentración de los reactivos.
- Gases: tienen la mayor velocidad de reacción debido a su alta energía cinética. La comprensión de gases aumenta las colisiones al reducir el volumen.
- Líquidos: tienen velocidades intermedias porque las partículas tienen menos libertad de movimiento.
- Solido: tienen las velocidades mas bajas debido a la limitada movilidad de sus partículas.
- Concentración: a mayor concentración de reactivos, aumentando la probabilidad de colisiones efectivas.

2. Grado de división: mayor la superficie de contacto entre los reactivos, mas colisiones ocurrirán.
3. Temperatura: al aumentar la temperatura las partículas adquieren mas energía cinética, lo que incrementa las colisiones y la velocidad.
4. Catalizadores: estos disminuyen la energía de activación, proporcionando rutas mas rápidas para la reacción.
Tipos de catalizadores:
- Catálisis homogénea
- Catálisis heterogénea
- Catálisis enzimática